QU’EST-CE QUE L’OXYDATION ?
L’oxydation est une réaction chimique entre atomes. Elle se rapporte à une perte d’électrons d’un atome au profit d’un autre qui devient l’oxydant. L’oxydant est souvent l’oxygène.
Dans le langage courant, on appelle « oxydation » le phénomène de corrosion, dû à l’oxygène présent dans l’air ou dans l’eau. La rouille est le résultat de l’oxydation du fer. Le fer cède ses électrons à l’oxygène (de l’air humide).
LE LIT DE LA VIE
L’oxydation est une réaction biochimique continuelle dans le corps pour la transformation des molécules (structure de base de la matière).
Tout est transformé dans le corps. Les aliments sont dégradés en molécules plus simples et servent à fournir de l’énergie.
La combustion des molécules alimentaires dans une cellule transforme les atomes de Carbone et d’Hydrogène riche en électrons (ou état réduit) en CO2 (gaz carbonique ou dioxyde de carbone) et H2O (eau), formes oxydées et plus stables. L’oxygène est très utilisé car il est contenu en grande quantité dans l’atmosphère terrestre.
En effet, il y a 3,5 milliards d’années, les êtres unicellulaires de la Terre se sont mis à consommer le gaz carbonique atmosphérique et à rejeter de l’oxygène par photosynthèse. Un milliard d’années après ce démarrage, l’oxygène, qui était sous forme de traces dans l’atmosphère primitive, a atteint 21% de l’air atmosphérique.
Dans la réaction d’oxydation chimique qui implique le carbone du glucose C6H12O6 et l’oxygène O2, par exemple, il y a formation de CO2, d’H2O et d’énergie. Les réactions d’oxydation fournissent de l’énergie aux cellules sous forme d’ATP qui sert à de nombreuses réactions métaboliques de l’organisme et à l’activité musculaire.
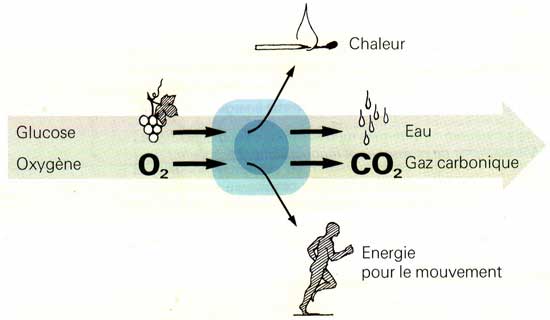
Bilan de l’oxydation du glucose (Paul Walder 1989)
LA VIE UTILISE L’OXYDATION : EXEMPLE DU PLANCTON
Des vagues lumineuses bleues en pleine nuit sur la côte californienne, côté Pacifique sont créés par le phytoplancton bioluminescent. La réaction chimique d’oxydation entre la molécule luciférine et l’enzyme luciférase crée de l’énergie transformée en lumière bleu.
L’émission de lumière de ces organismes unicellulaires leur permet d’être mieux vus des poissons dont le système digestif est un milieu plus favorable à leur développement que l’eau de mer.

Brian Mack/Handout via REUTERS
CONCLUSION
La réactivité de l’oxygène se traduit par de nombreuses réactions de transfert d’électrons (rédox) qui conduisent à la formation de produits très stables, tels que H2O (eau), CO2 (gaz carbonique), HNO3 (acide nitrique), H2SO4 (acide sulfurique) et H3PO4 (acide phosphorique).
L’oxygène inspiré est utilisé par la vie pour produire de l’énergie en quantité suffisante, nécessaire à tout mouvement et à toute transformation.